A Sociedade Brasileira de Pediatria (SBP), em parceria com a Sociedade Brasileira de Imunizações (SBIm) e a Sociedade Brasileira de Infectologia (SBI), emitiu na última sexta-feira (15) uma nota técnica conjunta sobre o sarampo. O texto chama a atenção para a doença que era considerada eliminada do Brasil e das Américas, mas que deu sinais de retorno no ano passado.
Como resultado das ações de vigilância, laboratório e imunizações, em 2016, o Brasil recebeu o certificado de eliminação da circulação do vírus do sarampo pela Organização Mundial da Saúde (OMS), declarando a região das Américas livre da doença. Em janeiro de 2018, no entanto, casos importados da Venezuela deflagraram surtos em Roraima e no Amazonas, onde a cobertura vacinal estava bem abaixo dos necessários 95%.
Em relação à faixa etária, em ambos os Estados, a maior taxa de incidência da doença está concentrada entre crianças de seis meses a quatro anos de idade. Outros casos foram registrados posteriormente no Rio Grande do Sul, em São Paulo, no Mato Grosso e no Rio de Janeiro.
“A presença do vírus em nosso território reforça a necessidade de esforços no sentido da vigilância epidemiológica ativa (notificação de casos suspeitos idealmente em 24 horas, investigação ágil, adequada coleta e envio das amostras), do bloqueio através da imunização e de ações para a homogeneização das coberturas vacinais entre crianças, adolescentes e adultos”, diz trecho da nota.
LEIA AQUI A ÍNTEGRA DA DOCUMENTO.
NOTIFICAÇÕES – Segundo a Portaria Nº 204, de 17 de fevereiro de 2016, do Ministério da Saúde, o sarampo é doença de notificação obrigatória, ou seja, incluso na Lista Nacional de Notificação Compulsória de doenças, agravos e eventos de saúde pública nos serviços de saúde públicos e privados em todo o território nacional.
Os casos suspeitos ou confirmados devem ser notificados a fim de manter a eliminação do sarampo, mediante uma vigilância epidemiológica sensível, ativa e oportuna, permitindo assim, medidas de controle pertinentes.
A nota técnica conjunta orienta os pediatras sobre como analisar os exames para casos suspeitos e o vínculo epidemiológico, em que todo o caso suspeito que tenha tido contato de um ou mais casos de sarampo confirmados por exame laboratorial, e que apresentou os primeiros sintomas da doença entre 7 e 18 dias da exposição ao contato.
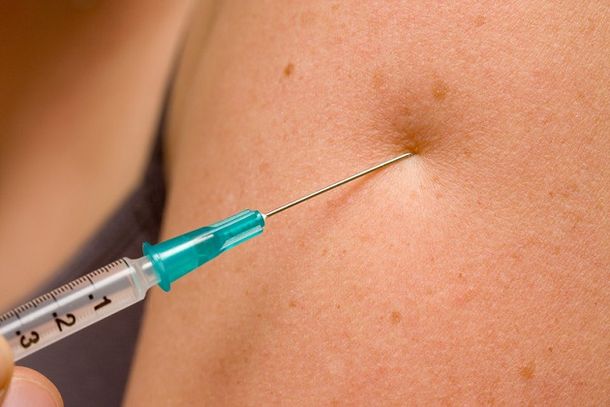
VACINAS – Na rede pública, são utilizadas vacinas tríplices virais (sarampo, caxumba e rubéola) de três diferentes laboratórios produtores, de acordo com as recomendações de bula e do Programa Nacional de Imunizações (PNI): Fiocruz/Bio-Manguinhos, Serum Institute of India Ltda. e GlaxoSmithkline Brasil Ltda. (GSK). Para crianças com menos de 5 anos, também está disponível a vacina tetra viral (sarampo, caxumba, rubéola e varicela), produzida pela GSK.
Na rede privada, estão disponíveis as vacinas tríplices virais (sarampo, caxumba e rubéola) e tetra virais (sarampo, caxumba, rubéola e varicela) de dois fabricantes: MSD e GSK.
De acordo com o Calendário de Vacinas da SBP e SBIm, a vacinação deve ser rotineira para crianças: duas doses aos 12 e 15 meses de idade, podendo ser realizada com as vacinas tríplice viral ou tetra viral. Crianças, adolescentes e adultos que não receberam essas doses na infância e que não tiveram sarampo, devem ser vacinados a qualquer momento: duas doses com intervalo mínimo de 30 dias entre elas.
BLOQUEIO DE SURTO – A nota técnica recomenta também que, diante de surtos, a vacinação de bloqueio é fundamental para o controle do mesmo, e deve ser iniciada o mais precocemente possível, preferencialmente até 72 horas após o contato. Daí a importância da notificação de casos suspeitos para que, além de iniciada a investigação do caso, possa ser instituída essa importante medida.
“Em situações de surto ou de contato com pessoa com suspeita de sarampo, lactentes a partir de 6 meses deverão ser vacinados. No entanto, essa dose não deverá ser considerada como válida, e, portanto, precisarão receber as doses dos 12 e 15 meses de idade”, destaca a nota.

PED CAST SBP | "Puericultura: entenda os marcos do desenvolviment...
25/11/2024 , 10:33
E-book relembra os 40 anos do Departamento de Saúde Escolar da SB...
25/11/2024 , 09:10
Volume 14, número 3, da revista RP já está disponível para leitur...
25/11/2024 , 09:07
Manual de seguimento do Recém-nascido de alto risco - 2ª edição
25/11/2024 , 08:34
Representante da SBP participa de 2º Simpósio sobre Doenças Crôni...
21/11/2024 , 14:53
Departamentos Científicos e Grupos de Trabalho da SBP apresentam ...
18/11/2024 , 12:16